Ingrese su ID de correo electrónico
FISIOLOGIA / SISTEMA DIGESTIVO / INTRODUCCIÓN AL APARATO DIGESTIVO
INTRODUCCIÓN AL ESTUDIO DEL APARATO DIGESTIVO
TABLA DE CONTENIDO
- Objetivos
- Significado biológico
- Aspectos morfofuncionales del sistema digestivo
- Circulación esplácnica
- Inervación del sistema digestivo
- Integración y control de la función digestiva
- Función interdigestiva (Complejo Motor Migratorio)
- Referencias
INTRODUCCIÓN SISTEMA DIGESTIVO
ES UN SISTEMA DE VASOS DISEÑADO PARA DISTRIBUIR LA SANGRE OXIGENADA POR TODO EL ORGANISMO. SALIENDO DEL CORAZÓN, VA DISMINUYENDO SU DIÁMETRO HASTA LLEGAR A LOS TEJIDOS, DONDE SE ENCUENTRAN LOS VASOS DE MENOR CALIBRE (LOS CAPILARES). TAMBIÉN EN ESE CAMINO VAN CAMBIANDO SUS PROPIEDADES ELÁSTICAS Y CONTRÁCTILES, QUE DEFINEN SU FUNCIÓN EN CADA SEGMENTO.
OBJETIVOS
- Describir las características generales del sistema digestivo humano y el por qué del mismo.
- Describir las características morfofuncionales del sistema digestivo.
- Describir las características funcionales del músculo liso gastrointestinal.
- Describir las características morfofuncionales de la circulación esplácnica.
- Describir las características morfofuncionales de la regulación nerviosa del sistema digestivo, extrínseca e intrínseca.
- Describir los tipos de sensaciones en el sistema digestivo.
- Describir las características de la regulación endocrina y paracrina del sistema digestivo.
- Describir las características del Complejo Motor Migratorio Interdigestivo.
SIGNIFICADO BIOLÓGICO
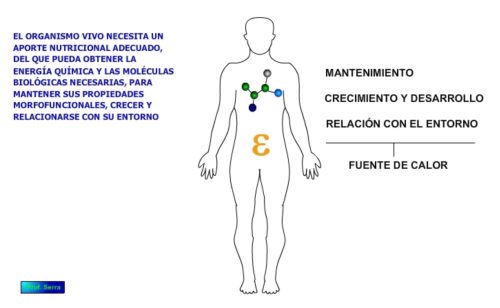
1. Para mantener las características morfofuncionales, crecer y relacionarse con el entorno, los seres vivos necesitan aporte continuo de energía. Este continuo aporte de energía, en su sentido más amplio lo podemos denominar NUTRICIÓN.
La vida constituye un continuo proceso de consumo de energía, con objeto de mantener el orden interno creado y de esa forma, contrarrestar las consecuencias de la segunda ley termodinámica, la cual nos indica que el Universo tiende al equilibrio, consistente en alcanzar el desorden máximo.
2. Los canales nutritivos son esencialmente tres:
a) de naturaleza química (formado por sustancias químicas y líquidas);
b) de naturaleza gaseosa (formada por los gases respiratorios);
c) de naturaleza electromagnética y mecánica (formada por las radiaciones y ondas que estimulan nuestros sentidos y constituyen la nutrición de nuestro sistema nervioso).
Atendiendo a la nutrición química, son tres los sustratos de los que los animales pueden obtener la energía necesaria para su metabolismo y crecimiento, así como algunas de las moléculas primarias implicadas en dicho metabolismo y crecimiento. Estos sustratos son hidratos de carbono, aminoácidos y lípidos, dentro de los cuales hay algunos que son esenciales porque el organismo no puede sintetizarlos. Además de éstos, el organismo también requiere de su entorno agua, minerales y algunas sustancias esenciales denominadas vitaminas.
El conjunto de todos estos materiales se encuentran en el entorno formando distintos tipos de agregados macromoleculares denominados ALIMENTOS. Éstos deben ser disgregados para convertirse en sus elementos moleculares simples, denominados NUTRIENTES. El sistema encargado de esta disgregación y favorecer su paso al interior del organismo (asimilación), es el SISTEMA DIGESTIVO.
La nutrición supone:
- Una conducta de búsqueda y captación de los alimentos,– Un sistema digestivo encargado de transformar los alimentos en elementos moleculares que puedan pasar la superficie que separa al medio externo digestivo del interno.
- Transportar los nutrientes a todos los rincones del sistema,
– Eliminar los materiales no utilizados en el proceso de la digestión,
– Integrar el proceso digestivo en el funcionamiento general del sistema vivo.
Los sistemas digestivos constan, en su mayoría, de un tubo que atraviesa antero posteriormente al organismo, con un polo oral en la región anterior por donde se ingieren los alimentos y, un polo anal, en la región posterior, por donde se eliminan los productos de desecho consecuentes al procesado fisicoquímico de los alimentos. Este canal digestivo (tracto digestivo o canal alimentario) alcanza en algunas especies varios metros de longitud (en el hombre más de diez), por lo que necesita de un sistema propulsor con la participación del músculo esquelético en su porción más inicial y final y de músculo liso en el resto, con lo cual se consigue la lenta progresión del bolo alimenticio a través del mismo. Estos movimientos están coordinados mediante un control neurógeno tanto intrínseco como extrínseco y un control hormonal y miogénico.
A lo largo de este canal o tracto alimentario se encuentran segmentos especializados en distintas funciones y en muchos casos, un mismo segmento presenta distintas funciones relacionadas con el procesado alimentario. Estas funciones son:
ingestión: captación y propulsión de los alimentos a través del tubo digestivo.
propulsión: movimientos generados por el componente muscular y regulados por un control neurogénico, hormonal y miogénico.
digestiva: (procesado de los alimentos)
fase mecánica: (movimientos mezclatorios y de trituración)
fase química: (reacciones enzimáticas de disgregación
secretora: (secreciones enzimáticas, hidrosalina y hormonal)
absortiba: (área especializada en el trasvase de nutrientes al torrente circulatorio)
intercambio: (donde se produce un equilibrio iónico e hídrico del contenido intestinal con la sangre)
defensiva: importante participación en el sistema inmune gracias a las características secretoras de algunas células intestinales y la presencia de las placas de Peyer ricas en linfocitos.
asimilación: utilización de los nutrientes por las células del organismo.
ESTRUCTURA DE LA PARED GASTROINTESTINAL
En la figura 5 se muestra la organización macroscópica del sistema digestivo.
La estructura histológica (Figura 6) del canal alimentario o tubo digestivo varía según la región que se estudie, pero básicamente consta de las siguientes capas:
1. capa serosa (adventicia), es la más externa y consta principalmente de tejido conectivo cubierto por una capa de células mesoteliales escamosas. Esta serosa se encuentra en todo el tracto digestivo excepto en el esófago, continuándose con el mesenterio, que contiene los nervios, vasos linfáticos y vasos sanguíneos del sistema.
2. capa muscular externa (muscularis propia), que consta de dos capas de células musculares lisas. Una capa circular interna y una capa longitudinal externa. En la región antral aparece otra capa intermedia oblicua. Entre ambas capas musculares se encuentra un importante plexo nervioso, el mientérico o de Auerbach, el cual coordina la actividad contráctil de la capa muscular externa y es responsable principal del mezclado y propulsión del contenido en la luz del tracto.
3. capa submucosa, que consta de tejido conectivo laxo con fibras de colágena y de elastina. En algunas regiones, se encuentran presentes glándulas submucosas. Por esta capa viajan los vasos sanguíneos más grandes, además de contener otro plexo nervioso, el submucoso o de Meissner.
4. capa mucosa, la más interna que consta de:
- un epitelio, cuya naturaleza y función varía según la zona del tracto digestivo,
- la lámina propia, que consta de tejido conectivo laxo que contiene fibras de colágena y elastina; es rica en distintos tipos de glándulas y contiene nódulos linfáticos y capilares.
- la muscular de la mucosa, que consta de dos capas delgadas de músculo liso, una circular interna y otra longitudinal externa. La contracción de esta capa muscular da la imagen característica de esta zona, como son los pliegues y surcos gastrointestinales que incrementan considerablemente la superficie de contacto entre los nutrientes y las secreciones gástricas, así como la superficie de absorción.
MÚSCULO LISO GASTROINTESTINAL
El músculo liso gastrointestinal pertenece a la categoría de músculo liso unitario o visceral, caracterizado por formar haces donde sus células musculares presentan entre sus membranas uniones de baja resistencia, que les da un comportamiento de sincitio funcional.
Estas células se encuentran inervadas por las terminales nerviosas de las neuronas entéricas y extrínsecas, con la particularidad de que no existen uniones neuromusculares tan bien definidas y específicas como en el músculo esquelético, sino que las terminales nerviosas presentan unas varicosidades distribuidas a lo largo de su longitud, con vesículas llenas de neurotransmisor y a una distancia media de unos 100 mm de las células musculares. Por lo que el neurotransmisor, una vez liberado, debe difundir hasta la membrana de la célula muscular.
El potencial de membrana en reposo de estas células es de aproximadamente unos -55 mV y aunque estable en condiciones aisladas, en el tejido muestra una oscilación periódica, determinada por la despolarización periódica de unas células próximas a las musculares y que se denominan intersticiales (estrelladas o de Cajal), las cuales actúan como células marcapasos del resto de las células musculares, con las que están en contacto. Este potencial viene determinado por corrientes lentas de calcio en la pendiente de subida, y de potasio en la de bajada.
Este potencial marcapaso lento es periódico y se propaga a lo largo del tracto gastrointestinal, dando lugar al RITMO ELÉCTRICO BÁSICO (REB), diferente en cada segmento. Así en el estómago es de 4/min; en el duodeno de 12/min; en el íleon de 8/min; en el ciego de 9/min y en el colon sigmoideo de 16/min.
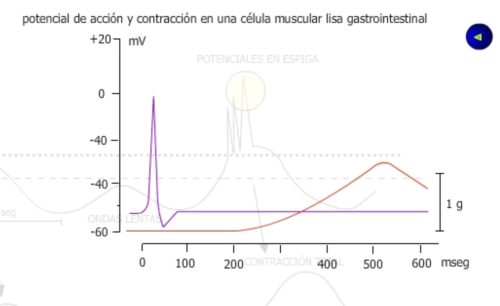
La célula muscular tiene un umbral eléctrico de excitabilidad y un umbral de contracción, lo que significa que cuando la onda de despolarización alcanza el umbral de contracción, se observa una contracción proporcional a la despolarización de la membrana (recuérdese que durante la despolarización está entrando iones calcio, necesarios para la contracción de los miofilamentos). Pero cuando se alcanza el umbral de excitabilidad, se puede observar como superpuestos a la onda de despolarización y en la pendiente ascendente de ésta, aparecen potenciales de acción con una frecuencia de 1 a 10 por segundo.
Cada potencial de acción genera una contracción, pero dado que la latencia de ésta con respecto al potencial de acción y la duración de la contracción es tan larga, las contracciones generadas por los diferentes potenciales de acción se suman.
Cuando cesa el estímulo contráctil, la tensión no vuelve a cero, ya que normalmente el músculo presenta un tono contráctil de reposo. Este tono se debe a la lentitud conque se retira el calcio iónico libre de la célula. En este tono participan tanto la liberación basal de neurotransmisores, como la presencia de las hormonas y factores humorales que actúan sobre la membrana de la célula muscular.
Tanto la amplitud (menos la frecuencia) de las ondas lentas, como la excitabilidad de las células musculares pueden ser moduladas por factores como los neurotransmisores, hormonas y factores humorales. Así la Ach aumenta el número de potenciales de acción y la tensión del músculo, mientras que las catecolaminas tienen un efecto contrario.
Hay dos propiedades características de este tipo de músculo liso que definen algunas características de la función gastrointestinal. La primera consiste en la propiedad de adaptación que tiene este tipo de músculo liso frente al estiramiento. Por la cual se pueden producir estiramientos lentos sin cambios importantes en la tensión. Sin embargo cuando el estiramiento es intenso, se produce una contracción reactiva, aunque cuando se mantiene dicho estiramiento se produce la relajación de la tensión.
CIRCULACIÓN ESPLÁCNICA
La sangre que riega al sistema digestivo viene de la arteria celiaca, la mesentérica superior y la inferior (figura 10). Los intestinos reciben de las dos últimas. Una de las principales características es el gran número de circulaciones paralelas que se desarrollan a nivel intestinal y subdivisiones hasta alcanzar las vellosidades intestinales donde su disposición permite el intercambio hidrosalino por mecanismos de contracorriente. La salida se realiza por la vena cava inferior. De los vasos localizados en la submucosa, salen ramas que irrigan a la capa muscula, la submucosa y la mucosa.
El hígado que representa el destino final de toda la absorción intestinal para su posterior procesado metabólico y distribución, recibe sangre de una rama de la celiaca, la arteria hepática, que suministra la sangre nutritiva para las células hepáticas y de la vena porta hepática, conocida como circulación enterohepática, por donde circula toda la sangre procedente de la absorción intestinal. Una característica de esta circulación es la denominada respuesta amortiguadora de la arteria hepática, consistente en un aumento o disminución del flujo sanguíneo de la arteria hepática recíproco al flujo sanguíneo portal. Este mecanismo parece estar controlado por la acción vasodilatadora en la circulación hepática de los metabolitos procedentes de la absorción que viajan por la circulación portal.
Hemodinámicamente hablando, el sistema digestivo recibe el 30% del GC, donde la mucosa recibe entre un 60 y 70% del flujo sanguíneo intestinal total (entre 70 – 100 ml/min/100gr). El hígado recibe alrededor de 1000 ml/min por la vena porta y 500 ml/min de la arteria hepática.
El sistema GI no regula de forma eficiente la resistencia (Figura 11), por lo que una disminución de la presión arterial supone una disminución del flujo sanguíneo, sin embargo la elevación de la presión venosa extraintestinal genera una vasoconstricción miogénica sostenida. Por otra parte la motilidad intestinal tiene poco efecto en el flujo sanguíneo, pero el incremento de la tasa metabólica durante la absorción si puede aumentar el flujo entre un 20 a un 80%. Igualmente la absorción de lípidos produce un aumento del flujo sanguíneo y consumo de oxígeno conocido como hiperemia absortiva, debida a la liberación de sustancias vasodilatadoras. La hiperosmolaridad también es un factor hiperémico importante.
Dentro del sistema GI, el flujo se distribuye por las vellosidades intestinales en forma de contracorriente. Esta disposición permite intercambios entre las arteriolas de entradas y las vénulas de salida que regulan en parte el gradiente osmolal (600 mOsm/Kg H2O en la punta y 400 mOsm/Kg H2O en la base) y la PO2 (menor en la punta). Estos gradientes aumentan considerablemente durante la absorción.
La regulación de este sistema se realiza por (Figura 12):
Sistema nervioso simpático, la activación de este sistema normalmente genera vasoconstricción mediada por los receptores a con reducción del flujo sanguíneo GI. (Ejercicio intenso, caída patológica de la presión arterial y el estrés, son factores que reducen el flujo sanguíneo GI.).
La autorregulación, determinada por factores metabólicos como la adenosina, el potasio, y la alteración de la osmolaridad.
La hiperemia funcional generada tras la ingestión de alimentos y producida por acción de las hormonas gastrointestinales (gastrina y colecistocinina) y algunos productos de la digestión como la glucosa y ácidos grasos libres de cadena ligera.
Los capilares subepiteliales presentan características propias que favorecen la absorción intestinal. Morfológicamente el endotelio presenta puntos de fusión entre sus membranas por falta de citoplasma (fenestraciones cerradas) por donde se favorece el paso de las sustancias absorbidas. También presentan un mayor coeficiente de filtración, además la presión sanguínea intestinal durante la absorción (13 a 20 mmHg) es menor que la presión coloidosmótica plasmática, favoreciéndose la absorción de agua. Efecto potenciado por la absorción de grasas (éstas disminuyen el coeficiente de reflexión de las proteínas (s)
INERVACIÓN DEL SISTEMA DIGESTIVO
La inervación del sistema digestivo se clasifica en dos categorías:
inervación intrínseca
inervación extrínseca
INERVACIÓN INTRÍNSECA
LA INERVACIÓN INTRÍNSECA (Figura 13), conocida también como “pequeño cerebro intestinal” ha sido diseñada para integrar y procesar la información gastrointestinal (GI) junto con la procedente del SNC, generando programas de acción GI. Por sus características funcionales se la considera como una tercera división del sistema nervioso denominándosele sistema nervioso entérico (SNE).
Posee neuronas sensoriales, interneuronas y neuronas efectoras de acción motora y secretora. El número de neuronas de este sistema es similar al existente en la medula espinal. Estas neuronas se agrupan en ganglios entéricos, cuya morfología, función y transmisores son diferentes a los simpáticos.
Existen dos grandes plexos ganglionares intramurales:
El Mientérico o de Auerbach localizado entre las capas musculares longitudinal y circular, en disposición plana, formando sus neuronas una única capa en el ganglio. Las neuronas controlan ambas capas musculares. De estos ganglios salen fibras C amielínicas (0,5 mm) que corren por la superficie muscular, adentrándose algunas en las capas musculares.
El Submucoso o de Meissner localizado entre la mucosa y la capa de músculo circular, en el espacio submucoso. Presenta ganglios más pequeños y con menos neuronas, siendo abundante en el ID e IG, inervando criptas y vellosidades.
Existe conexión entre ambos plexos, además de recibir información activadora e inhibitoria parasimpática (vagal) e inhibitoria simpática (Figura 14).
Las fibras procedentes de estos plexos que recorren todo el segmento GI forman los denominados plexos aganglionares, ubicados en otros planos de la pared gastrointestinal. En el fundus entre capa muscular circular y oblicua, en el intestino en la capa circular, en el colon en la superficie submucosa de la capa circular y en la lámina propia de todos los segmentos.
En estos ganglios se distinguen tres tipos morfológicos de neuronas, identificadas por Dogiel (D1,D2 y D3)[1]Dogiel tipo I: somas con prolongaciones cortas (dendritas) en forma de mazo y una única prolongación larga (axón) que puede atravesar varias filas de ganglios. (máximo 2 a 3 cm). Algunas (las más largas) son In; otras son Mn que atraviesan la capa muscular o mucosa. Se encuentran en ambos plexos.Dogiel tipo II: Somas lisos con prolongaciones cortas y largas las cuales pueden cruzar varias filas de ganglios orientándose en todas direcciones.Dogiel tipo III: … Continúe leyendo
, además de neuronas postganglionares parasimpáticas, células de mantenimiento, etc.
Desde el punto de vista neurofisiológico, son neuronas similares a las del SNC, con un Vm determinado por los iones potasio y un valor de -90 mV. Se distinguen dos tipos de neuronas:
Las S/Tipo1 (Hirst/North) son neuronas con Vm bajo, alta resistencia y alta excitabilidad que permite descargas repetitivas dependientes de sodio. Son neuronas con múltiples potenciales postsinápticos excitadores rápidos. Morfológicamente son Doguiel tipo I.
Las AH/Tipo 2 (Hirst/North) son neuronas con Vm > que las anteriores, menor resistencia y menor excitabilidad, generando pocas descargas dependientes de calcio. Sin embargo la convergencia temporal de neurotransmisores reguladores de calcio y estímulos despolarizantes determinan un importante incremento de su excitabilidad.
El potencial de acción de estas neuronas se caracteriza por una fase de hiperpolarización larga (varios segundos) que puede aumentar si coinciden dos potenciales de acción seguidos, reduciéndose su excitabilidad (por incremento del periodo refractario). Estas características dependen de canales de calcio dependientes de voltaje y canales de potasio dependientes de calcio.
Morfológicamente son neuronas Dogiel tipo II y III. Se encuentran en ambos plexos, aunque no en el cuerpo del estómago.
Son más de 20 los neurotransmisores implicados en el sistema entérico, entre ellos destacamos: los transmisores putativos no peptídicos: ACh, NA, ATP, adenosina, serotonina, dopamina, GABA, histamina, glicina y prostaglandinas. Los de carácter peptídico: sustancia P, VIP (péptido intestinal vasoactivo), GRP (péptido liberador de gastrina), encefalina, somatostatina, CCK, secretina, neurotensina, motilina, gastrina, hormona liberadora de tirotrofina, angiotensina y neuropéptido Y.
Algunas Dogiel tipo I poseen 5HT en sus terminaciones largas orientadas en dirección oral, concentrada en las varicosidades axónicas. Otras tienen VIP y óxido nítrico proyectándose en dirección aboral por un espacio corto antes de girar y entrar en la capa muscular circular. Son Mn inhibidoras del músculo circular.
Otras tipo I del plexo submucoso tienen VIP y acetilcolina, siendo excitadoras e inervando las criptas intestinales, son neuronas secretomotoras. También hay neuronas tipo I en plexo mientérico con sustancia P y acetilcolina, siendo Mn excitadoras de la pared GI.
Las Dogiel tipo II y III contienen sustancia P y son In.
Además de estas neuronas hay otras células, células intersticiales de Cajal, ubicadas en los plexos aganglionares, entre las capas musculares longitudinal y circular y en la submucosa, formando redes y especializadas en la generación de las ondas lentas de despolarización características del sistema GI.
INERVACIÓN EXTRÍNSECA
La inervación extrínseca (Figura 16) está formada por las ramas simpáticas y parasimpáticas del sistema nervioso autónomo.
La inervación parasimpática proviene principalmente del vago y de los nervios pelvianos. Estas fibras parasimpáticas son preganglionares y sinaptan con las células de los plexos entéricos, por lo tanto no son fibras nerviosas motoras comunes. Su función es la de aumentar o disminuir la excitabilidad de los centros nerviosos entéricos. El neurotransmisor es la Acetilcolina a través de receptores nicotínicos con las neuronas postganglionares y muscarínicos en su acción sobre la fibra muscular lisa.
El vago inerva el tracto digestivo desde el esófago hasta el colon transverso. Los somas neuronales de estas fibras vagales se encuentran en el bulbo, unos en el núcleo ambíguo encargado de controlar la musculatura voluntaria de la región faringeoesofágica. Otros en el núcleo dorsal motor del vago, del que parten fibras motoras, secretoras y vasodilatadoras dirigidas a los órganos cardiopulmonares y esofagoabdominales. No obstante, la mayor proporción de fibras son de tipo sensorial. Las fibras sensoriales vagales que nacen en el sistema digestivo, proceden de receptores tipo mecanoceptores, quimioceptores y osmoceptores y son amielínicas, realizando la primera sinápsis en el núcleo del tracto solitario. La información procesada en el bulbo genera una respuesta motora vagal, denominándose reflejo vagovagal.
Las eferencias vagales preparan al sistema digestivo ante un proceso digestivo y posteriormente participan en la coordinación GI. Ejercen efectos excitatorios e inhibitorios según la región afectada. (Ej.: + secreción y paralelamente relajación del esfínter esofágico inferior por inhibición.)
La inervación simpática se establece por vía de los nervios esplácnicos de los plexos celíacos, mesentérico superior e inferior e hipogástrico. Estas fibras son postganglionares y en su mayor parte noradrenérgicas. Inervan principalmente a los vasos sanguíneos gastrointestinales y a las neuronas de los plexos intramurales y a las células glandulares, aunque algunas fibras inervan la capa muscular de la mucosa, originando las características rugosidades intestinales. El neurotransmisor es la noradrenalina a través de receptores a2 y b. La acción simpática es una inhibición presináptica de la célula efectora.
Las fibras sensoriales simpáticas se originan en receptores próximos a los vasos sanguíneos mesentéricos y son de tipo mecanoceptoras y dolorosas. También parten del sistema nervioso entérico fibras sensoriales mecanoceptoras que sinaptan con neuronas de los ganglios prevertebrales, de donde parte la respuesta efectora hacia el sistema GI. Esta disposición permite la coordinación simpática de distintos segmentos GI, ya que la propia del sistema GI es muy lenta por el número de sinápsis interpuestas, siendo la base de los reflejos enteroentéricos (distensión de una región GI genera inhibición motora en otra región GI alejada).
SENSACIONES VISCERALES EN EL SISTEMA DIGESTIVO
Las sensaciones viscerales que se originan en el sistema digestivo (Figura 17) son de tacto sólo en la parte inferior de la faringe. Temperatura normalmente en el extremo inferior del esófago, el ano y la mucosa gástrica cuando las temperaturas son < a 1º y > a 45º. En la sensación a productos químicos sólo el alcohol produce respuesta en la mucosa gástrica, y en el ano junto a la glicerina.
La sensación de dolor tiene tres componentes: dolor visceral cuyos receptores son corpúsculos de Pacini y terminaciones nerviosas libres en la pared visceral, sensibles al espasmo visceral y a la distensión (estiramiento). Las fibras viajan por el esplácnico aferente. Dolor somático procedente del peritoneo anterior de la cavidad abdominal, epiplon menor, mesenterio y mesocolon, a través de los nervios cerebroespinales (B6-B12). Dolor referido, generado por la confluencia de las fibras sensoriales viscerales y somáticas en cada segmento espinal, lo que determina la aparición de dolor dérmico en la región dérmica inervada por dicho segmento.
La distensión (estiramiento) es el principal estímulo doloroso. Producido en el estómago y/o porción inferior del esófago, se produce la sensación de náusea. Los cambios de aceleración en los ascensores son un ejemplo de estiramiento del esófago que determinan sensación de náusea.
INTEGRACIÓN Y CONTROL DE LAS FUNCIONES DIGESTIVAS.
CONTROL NEURÓGENO
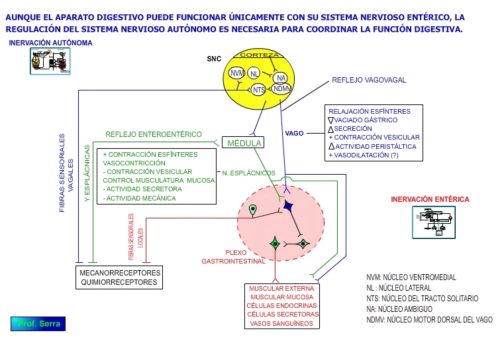
El control neurógeno (Figura 18) procedente del SNE es esencial para coordinar la actividad entre los distintos segmentos del sistema digestivo, de hecho el sistema digestivo puede funcionar sin inervación extrínseca, no obstante esta última inervación es importante a la hora de modular la respuesta general del sistema digestivo, así como de conectar su funcionamiento con el funcionamiento general del sistema vivo.
A nivel hipotalámico, hay núcleos que están implicados en el control del sistema digestivo, destacando el hipotálamo anterior, donde el núcleo ventromedial está implicado en el control de la saciedad y como sensor glucémico sanguíneo, controlando también la motilidad gástrica. El núcleo lateral controla la secreción gástrica y se encuentra en estrecha relación con el ventromedial, su lesión determina la aparición de una afagia (pérdida del apetito). Fibras sensoriales vagales y simpáticas, sensitivas a la glucosa intestinal y portal mandan información a estos núcleos, de forma que la disminución de glucosa supone que el hipotálamo excite a células de los núcleos del vago para incrementar la secreción ácida y las contracciones antrales. De acuerdo con Moore (1980), la variación en la secreción basal de ácido durante 12 horas, está en relación inversa a la concentración de glucosa en sangre.
La estimulación eléctrica parasimpática, produce salivación (nervios VII y IX), en el vago aumenta la actividad peristáltica, la relajación de los esfínteres intestinales, la disminución del vaciado gástrico y el aumento en la secreción de gastrina y otros jugos digestivos, contrae la vesícula biliar, produce la secreción de los jugos pancreáticos y la liberación de insulina. La estimulación de los nervios pelvianos, ocasiona relajación de esfínteres anales de tipo esquelético.
La estimulación eléctrica de las fibras simpáticas entéricas ocasionan vasoconstricción, inhiben la contracción de la vesícula biliar, la actividad mecánica y secretora del estómago e intestinos y contraen los esfínteres intestinales, etc. Es decir, disminuyen el estado de contracción y activan la contracción de los esfínteres.
Veremos como en la regulación nerviosa del tracto gastrointestinal, normalmente ésta se produce en dos fases fundamentales: una inicial denominada cefálica, o de anticipación al proceso digestivo. Con ésta y mediada por el sistema nervioso autónomo, se prepara al sistema digestivo para recibir y digerir el bolo alimenticio. Después le sigue una fase propiamente entérica, donde la estimulación de los sensores entéricos, en función de la composición y características físico-químicas del bolo alimenticio, genera una serie de respuestas reflejas intrínsecas capaces de coordinar los diferentes procesos digestivos en los diferentes segmentos.
INTEGRACIÓN Y CONTROL DE LAS FUNCIONES DIGESTIVAS.
CONTROL HORMONAL Y PARACRINO
El sistema digestivo se caracteriza por ser un prolífico secretor de hormonas y factores humorales, por este motivo podemos clasificar este control en: control hormonal entérico, control paracrino y control hormonal periférico.
Muchas de las células que forman la mucosa gastrointestinal tienen capacidad de producir y secretar hormonas y factores humorales ante estímulos directos del contenido gastrointestinal, así como por acción del control neurógeno. Muchas de estas células además en su liberación hormonal hacia el torrente sanguíneo, se produce difusión hacia los espacios intercelulares próximos por lo que pueden ejercen una acción paracrina. Por esta razón es difícil hacer una clasificación de las hormonas y factores paracrinos. Algunos de éstos son claramente hormonas, por ejercer su acción principalmente a través del torrente circulatorio, sin embargo también están presentes en terminaciones nerviosas entéricas e incluso como factores paracrinos.
Entre estos compuestos hormonales entéricas y factores paracrinos podemos destacar por su papel probado: la gastrina, colecistocinina-pancreomicina (CCK), la secretina, el péptido inhibidor gástrico (GIP), el péptido intestinal vasoactivo (PIV), el polipéptido liberador de gastrina (PLG), la motilina, somatostatina, histamina, la serotonina, la neurotensina, el polipéptido pancreático y el péptidoYY. (Fgura 19)
El control hormonal periférico viene determinado por hormonas tiroideas, insulina, glucagón, hormona del crecimiento y cortisol en lo referente a regulación metabólica y circadiana. En la regulación hídrica (en el sistema digestivo hay importantes movimientos de agua) la aldosterona.
Hay claras evidencias de que la ingestión de alimentos está sujeta a un ritmo circadiano circanual, frente a la presencia permanente de alimentos. Por otro lado, también se han comprobado cambios bioperiódicos en la absorción y metabolismo de los nutrientes, cambios que están ligados a procesos cronofisiológicos de tipo hormonal y enzimático entre otros. Así por ejemplo, Fisher y Gardner han demostrado que la absorción intestinal de glucosa, está sujeta a un ritmo circadiano (al menos en la rata). Así mismo, Apfelbaum y Reinberg han demostrado la persistencia de un ritmo circadiano en el cociente respiratorio en el transcurso de una dieta exclusivamente proteica y prolongada, con un incremento de la neoglucogénesis en unas horas y la glicólisis en otras. Estos cambios son consecuencia probablemente de hormonas como la de crecimiento, glucagón, insulina, cortisol, etc, lo cual nos indica que las vías metabólicas de los nutrientes no se abren al mismo tiempo ni de la misma manera, pudiéndose observar que en individuos de actividad diurna, la glicólisis predomina por la mañana, mientras que al anochecer predominan las vías metabólicas de almacenamiento energético. Las experiencias de Halberg en estos aspectos son claras, por cuanto ante el suministro de una solo comida, los individuos que la realizaban por la mañana perdían peso, mientras que los que la realizaban por la noche, incrementaban de peso.
FASE INTERDIGESTIVA. COMPLEJO MOTOR MIGRATORIO (CMM)
Se conoce con tal término al patrón motor que puede observarse en el tracto gastrointestinal durante la fase interdigestiva, es decir durante el periodo de ayuno. Abarca desde el estómago hasta el final del ID.
Este patrón motor se inicia en el estómago y progresa hasta el íleo distal a una velocidad de 5cm/min (aunque ésta disminuye a medida que se aproxima al íleon) y una periocidad de aproximadamente unos 90 minutos. Este patrón desaparece en el momento que se produce la ingesta y se reanuda nuevamente, a los 90 a 120 minutos después de finalizada la digestión.
Consta de tres fases:
La fase I es de quietud electromecánica, larga duración (unos 70 minutos (40-60% del ciclo)) y secreción hidrosalina, seguida de la fase II caracterizada por una actividad electromecánica irregular con potenciales en espiga y contracciones irregulares, con secreción de tipo enzimática y una duración aproximada de unos 15 minutos (no hay impulso del contenido luminal) (dura 20-30% del total); terminando con la fase III, donde se produce una importante actividad electromecánica con potenciales en espiga y contracciones regulares de 11 a 13/minuto con una duración de 1 a 5 minutos que si impulsan el contenido luminal hacia delante.
Hay apertura total del píloro que permite la evacuación de los agregados no digeridos (abezoares). También hay apertura del esfínter de Oddi y aumento de la secreción intestinal y órganos anejos.
La función de este complejo puede ser la de limpieza del tracto gastrointestinal entre comidas, ya que se produce secreción hidrosalina y enzimática, además de propulsión del líquido secretado y restos hacia la válvula ileocecal.
En su origen están implicados tanto factores humorales (motilina) como nerviosos; y en su transformación al patrón digestivo, están implicadas las hormonas gastrointestinales que se producen en la fase digestiva. El tiempo de inhibición del CMMI depende de la ingesta calórica (sobre todo de la absorción calórica) y a igual ingesta calórica depende del tipo de nutriente, así las grasas retardan el CMMI más que los glúcidos y éstos más que los prótidos.
Aunque se paralice el sistema autónomo, hay fase III del CMM y sí hay un aumento plasmático de MOTILINA, cuya liberación se inhibe con la ingesta. La motilina favorece la liberación de Ach, 5HT y NO.
El vago amplifica esta respuesta. La inhibición del vago elimina la fase II.
La acción central se observa en la variación circadiana de este patrón y disminuye durante el sueño. El estrés reduce los ciclos del MMC mediante la liberación del CRF y la activación de una vía vagal colinérgica.
Además de limpieza parece evitar el reflujo del colon hacia el ID, como se observa en pacientes en los que se interrumpe el MMC, llenándose el ID de bacterias.
ENLACES DEL TEMA EN LA WEB
Sistema nervioso entérico (wikipedia)
Sistema nervioso entérico y motilidad gastrointestinal
YOUTUBE
Sistema nervioso entérico. Estructura y función. (Dr. Rafael Estrada)
PATOLOGÍAS
Enfermedades difusas del sistema nervioso entérico.
Sistema nervioso entérico y enfermedad inflamatoria intestinal.
FISIOLOGIA / SISTEMA DIGESTIVO / INTRODUCCIÓN AL APARATO DIGESTIVO
![]()


















 Views Today : 167
Views Today : 167 Views This Month : 15266
Views This Month : 15266 Views This Year : 30044
Views This Year : 30044 Total views : 399191
Total views : 399191